2.2. La revolución en el tratamiento del VHC
Desde la aparición del primer tratamiento con actividad para el VHC en el año 1991 (interferón-alfa; IFN-alfa) hasta la actualidad, el tratamiento del VHC ha sufrido una evolución espectacular (Figura 4). Durante más de 10 años, hasta el 2011 el tratamiento consistía en la combinación de interferon pegilado (PEGIFN) por vía subcutánea y ribavirina (RBV) por vía oral durante 24-48 semanas, según el genotipo. Sin embargo, estos tratamientos tenían una eficacia limitada (hasta el 50% en genotipo 1) y un mal perfil de efectos adversos (anemia, neutropenia, depresión)17,18 .
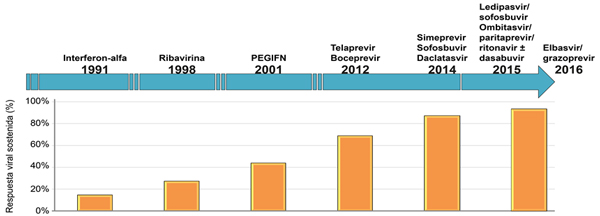
Figura 4. Años de aparición de los antivirales del VHC y la evolución de los % de RVS.
Gracias al avance en el conocimiento del ciclo vital del VHC y de las características estructurales de las proteínas del virus, se han podido diseñar nuevos fármacos. Los antivirales de acción directa (AAD) actúan de forma específica sobre una o varias partes del ciclo de vida del virus rompiendo así la cadena de reproducción. Las principales dianas terapéuticas son la proteasa NS3/4A, la polimerasa NS5B y el complejo de replicación NS5A del VHC.
En 2012 se comercializaron los primeros AAD, los inhibidores de la proteasa (IP) telaprevir (TPV) y boceprevir (BOC). La administración de estos IP asociados a PEGIFN y RBV (denominada Triple Terapia), con indicación únicamente en el genotipo 1, mejoraba la tasa de RVS hasta un 70% en pacientes sin tratamiento previo (naïve)19.20. Sin embargo, producían reacciones adversas graves, requiriendo seguimiento más estrecho del paciente y una monitorización frecuente de la carga viral para valorar la necesidad de continuación de tratamiento, al tener establecidas “reglas de parada”.
El año 2014 fue trascendental para los pacientes infectados por el VHC. Se autorizaron tres nuevos AAD (sofosbuvir, simeprevir y daclatasvir) para su utilización, tanto combinados con PEGIFN, como asociados con otros AAD en regímenes de administración oral. En 2015 aparecieron los primeros antivirales co-formulados, combinando diferentes AAD en un mismo comprimido. Las combinaciones de AAD sin PEGIFN lograron aumentar las tasas de RVS a valores antes inimaginables, llegando a superar el 90%.
